Die im Folgenden zitierte Studie lässt ein signifikant erhöhtes Risiko besonders bei jüngeren Menschen erkennen, an einer Herzerkrankung zu leiden oder zu sterben, die sich mehrfach mit einem mRNA-Impfstoff haben impfen lassen.
Die übersetzten Auszüge dieses Beitrags sind im Original erstmals am 14. Dezember 2021 Online auf der Seite des Magazins Nature erschienen
Published: 14 December 2021
Risks of myocarditis, pericarditis, and cardiac arrhythmias associated with COVID-19 vaccination or SARS-CoV-2 infection
Martina Patone,
Xue W. Mei,
Lahiru Handunnetthi,
Sharon Dixon,
Francesco Zaccardi,
Manu Shankar-Hari,
Peter Watkinson,
Kamlesh Khunti,
Anthony Harnden,
Carol A. C. Coupland,
Keith M. Channon,
Nicholas L. Mills,
Aziz Sheikh &
Julia Hippisley-Cox
Abstrakt
Obwohl Myokarditis und Perikarditis in den Impfstoffstudien zur Coronavirus-Krankheit 2019 (COVID-19) nicht als unerwünschte Ereignisse beobachtet wurden, gab es zahlreiche Berichte über Verdachtsfälle nach Impfungen in der Allgemeinbevölkerung. Wir haben zwischen dem 1. Dezember 2020 und dem 24. August 2021 in England eine selbstkontrollierte Fallserienstudie mit Personen im Alter von 16 Jahren oder älter durchgeführt, die in England gegen COVID-19 geimpft wurden, um die Krankenhauseinweisung oder den Tod durch Myokarditis, Perikarditis und Herzrhythmusstörungen in den 1–28 Tagen zu untersuchen Adenovirus (ChAdOx1, n = 20.615.911) oder Messenger-RNA-basierter (BNT162b2, n = 16.993.389; mRNA-1273, n = 1.006.191) oder ein schwerer akuter respiratorischer Syndrom Coronavirus 2 (SARS-CoV-2) positiver Test (n = 3.028.867 .) ).
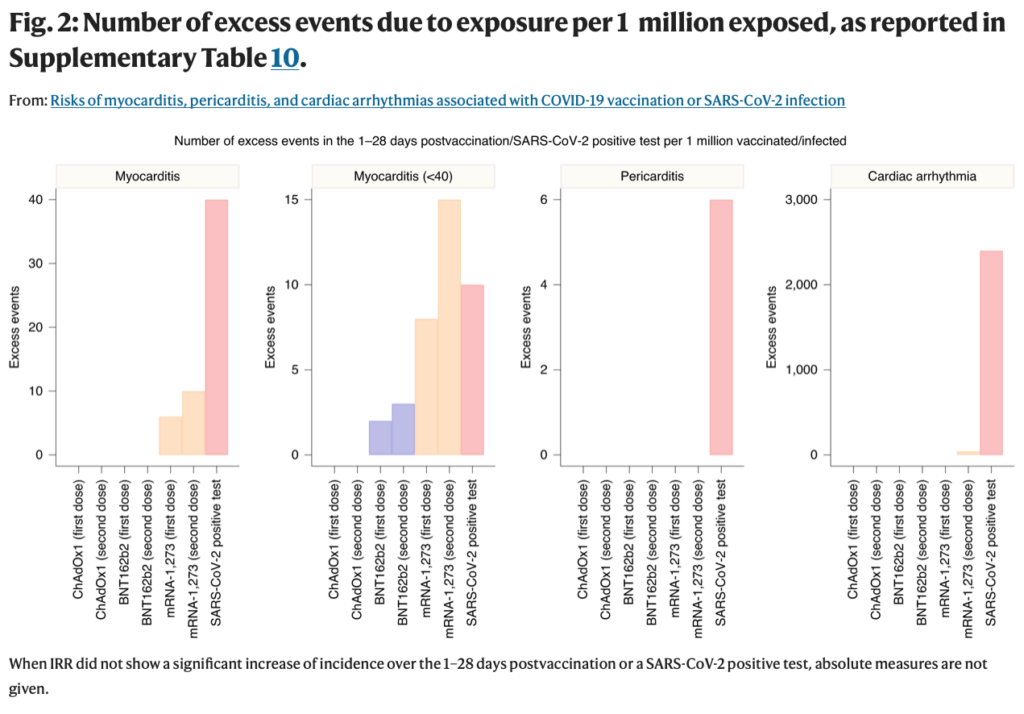
Wir fanden ein erhöhtes Myokarditisrisiko im Zusammenhang mit der ersten Dosis der Impfstoffe ChAdOx1 und BNT162b2 sowie der ersten und zweiten Dosis des Impfstoffs mRNA-1273 über den Zeitraum von 1–28 Tagen nach der Impfung und nach einem positiven SARS-CoV-2-Test. Wir schätzten zwei zusätzliche (95 %-Konfidenzintervall (KI) 0, 3), ein (95 %-KI 0, 2) und sechs (95 %-KI 2, 8) Myokarditis-Ereignisse pro 1 Million Personen, die mit ChAdOx1, BNT162b2 und mRNA geimpft wurden -1273 in den 28 Tagen nach einer ersten Dosis und weitere zehn (95% CI 7, 11) Myokarditisereignisse pro 1 Million Geimpften in den 28 Tagen nach einer zweiten Dosis mRNA-1273.
Dies vergleicht sich mit zusätzlichen 40 (95% CI 38, 41) Myokarditis-Ereignissen pro 1 Million Patienten in den 28 Tagen nach einem positiven SARS-CoV-2-Test. Wir beobachteten auch ein erhöhtes Risiko für Perikarditis und Herzrhythmusstörungen nach einem positiven SARS-CoV-2-Test. Ähnliche Assoziationen wurden bei keinem der COVID-19-Impfstoffe beobachtet, abgesehen von einem erhöhten Risiko für Herzrhythmusstörungen nach einer zweiten Dosis von mRNA-1273. Subgruppenanalysen nach Alter zeigten, dass das mit den beiden mRNA-Impfstoffen verbundene erhöhte Myokarditisrisiko nur bei Personen unter 40 Jahren bestand.
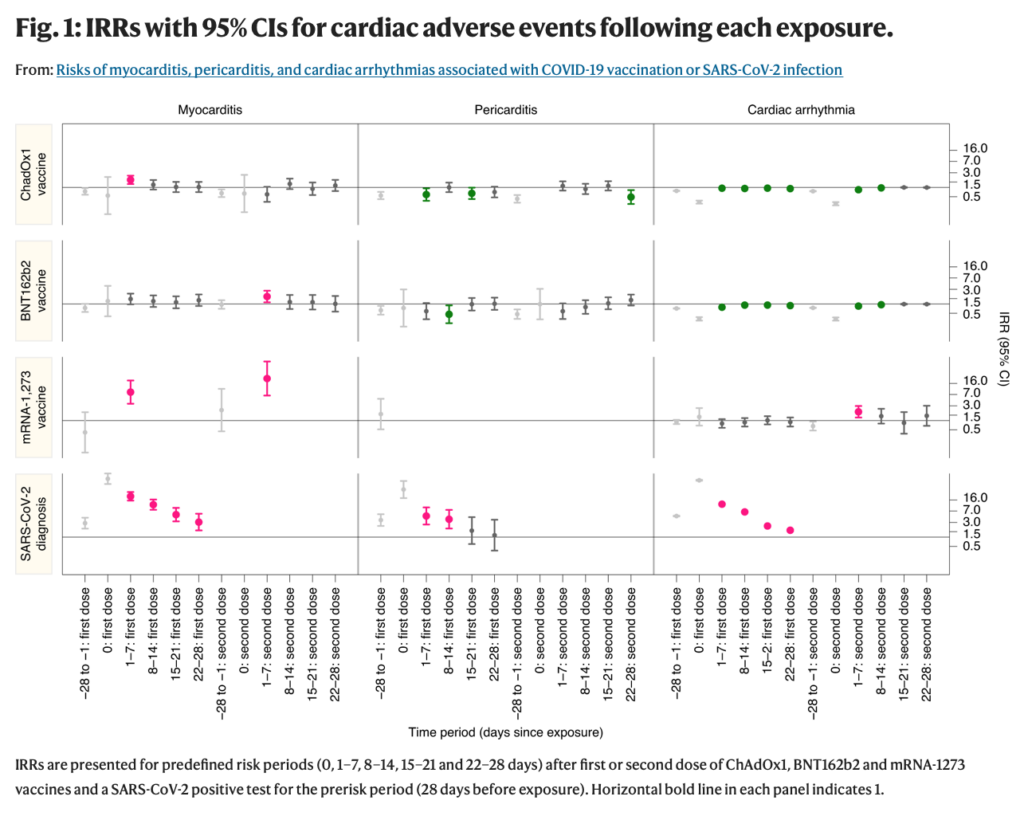
Myokarditis
Myokarditis
Von den 38.615.491 geimpften Personen, die in unsere Studie eingeschlossen wurden, wurden 1.615 (0,004 %) zu irgendeinem Zeitpunkt im Studienzeitraum (entweder vor oder nach der Impfung) mit Myokarditis ins Krankenhaus eingeliefert oder starben daran; 397 (0,001%) davon traten in den 1-28 Tagen nach jeder Impfung auf. Von den 1.615 Eingelieferten oder Verstorbenen hatten 359 (22,2%) einen SARS-CoV-2-positiven Test, davon 287 (17,8%) vor der Impfung.
Es wurden 114 Todesfälle mit Myokarditis als Todesursache auf der Sterbeurkunde verzeichnet (23 hatten einen positiven SARS-CoV-2-Test). Von denjenigen, die in den 1-28 Tagen nach der Impfung mit Myokarditis aufgenommen wurden oder daran starben, hatten 12,7 % (18) und 10,7 % (9) einen positiven SARS-CoV-2-Test vor der ersten und zweiten Dosis des ChAdOx1-Impfstoffs. bzw. 7,4 % (7) vor der ersten Dosis des BNT162b2-Impfstoffs (Tabelle 2).
1-7 Tage nach der ersten Dosis von ChAdOx1 (IRR 1,76; 95 %-KI 1,29, 2,42), BNT162b2 (IRR 1,45, 95 %-KI 0,97, 2,12) und mRNA-1273 (IRR 8,38, 95 %-KI 3,53, 19,91) und die zweite Dosis von BNT162b2 (IRR 1,75, 95 %-KI 1,13, 2,70) und mRNA-1273 (IRR 23,10, 95 %-KI 6,46, 82,56). Es bestand ein erhöhtes Myokarditisrisiko nach 1–7 Tagen (IRR 21,08, 95 % KI 15,34, 28,96), 8–14 Tage (IRR 11,29, 95 % KI 7,70, 16,57), 15–21 Tagen (IRR 5,36, 95 % CI 3,24, 8,89 und 21–28 Tage (IRR 3,08, 95 % CI 1,65, 5,75) nach einem positiven Test.
Über die 1–28 Tage nach der Impfung beobachteten wir eine Assoziation mit der ersten Dosis von ChAdOx1 (IRR 1,29, 95 % KI 1,05; 1,58), BNT162b2 (IRR 1,31, 95 % KI 1,03, 1,66) und mRNA-1273 (IRR 2,97; 95 %-KI 1,34, 6,58). Nach einer zweiten Dosis war das erhöhte Risiko bei mRNA-1273 (IRR 9,84, 95 % KI 2,69, 36,03) viel höher als bei BNT162b2 (IRR 1,30, 95 % KI 0,98, 1,72). Das Myokarditisrisiko war in den 1–28 Tagen nach einem positiven SARS-CoV-2-Test erhöht (IRR 9,76, 95 % KI 7,51, 12,69).
Perikarditis
Von den 38.615.491 geimpften Personen, die in unsere Studie eingeschlossen wurden, wurden 1.574 (0,004 %) zu irgendeinem Zeitpunkt im Studienzeitraum (entweder vor oder nach der Impfung) mit Perikarditis ins Krankenhaus eingeliefert oder starben daran; 356 (0,001%) davon traten in den 1-28 Tagen nach einer Impfdosis auf.
Von den 1.574 Eingelieferten oder Verstorbenen wiesen 188 (11,9%) einen positiven SARS-CoV-2-Test auf, davon 154 (9,8%) vor der Impfung. Als Todesursache wurden 31 Todesfälle mit Perikarditis auf der Sterbeurkunde verzeichnet (6 hatten einen positiven SARS-CoV-2-Test). Tabelle 2 zeigt die Prozentsätze der Patienten mit Perikarditis-Ereignissen im Risikozeitraum, die vor der Impfung einen positiven SARS-CoV-2-Test aufwiesen, nach Impfstofftyp und -dosis.
Nach einer ersten Dosis von ChAdOx1 (IRR 0,59; 95 %-KI 0,37, 0,94 nach 1–7 Tagen, IRR 0,64; 95 %-KI 0,42, 0,99 nach 15–21 Tagen) von BNT162b2 (IRR 0,46; 95 %-KI 0,24, 0,90 nach 8–14 Tagen) und nach einer zweiten Dosis ChAdOx1 (IRR 0,49; 95 %-KI: 0,29, 0,82 nach 22–28 Tagen). Es gab nicht genügend Ereignisse, um die Assoziation mit dem mRNA-1273-Impfstoff pro Woche zu bewerten. Es bestand ein erhöhtes Risiko einer Krankenhauseinweisung oder eines Todesfalls aufgrund einer Perikarditis nach 1–7 Tagen (IRR 4,85, 95 % KI 2,56; 9,18) und 8–14 Tage (IRR 3,81, 95 % KI 1,90; 7,63) nach einem SARS-CoV- 2 positiver Test.
Über die 1–28 Tage nach der Impfung beobachteten wir ein verringertes Risiko einer Perikarditis nach der ersten Dosis von ChAdOx1 (IRR 0,74, 95 % KI 0,59; 0,92), im Gegensatz zu einem erhöhten Risiko in den 1–28 Tagen nach einem SARS-CoV -2 positiver Test (IRR 2,79, 95% CI 1,80, 4,32). Es wurde keine Assoziation mit dem BNT162b2- oder mRNA-1273-Impfstoff beobachtet.
Herzrhythmusstörungen
Von den 38.615.491 geimpften Personen, die in unsere Studie aufgenommen wurden, wurden 385.508 (1,0 %) zu irgendeinem Zeitpunkt im Studienzeitraum (entweder vor oder nach der Impfung) mit Herzrhythmusstörungen ins Krankenhaus eingeliefert oder starben daran; 86.754 (0,2%) davon traten in den 1-28 Tagen nach einer Impfdosis auf.
Von den Eingewiesenen oder Verstorbenen hatten 39.897 (10,3%) einen positiven SARS-CoV-2-Test, 29.694 (7,7%) einen positiven Test vor der Impfung. Es gab 7.795 Todesfälle mit Herzrhythmusstörungen als Todesursache (1.108 hatten einen positiven SARS-CoV-2-Test). Tabelle 2 zeigt die Prozentsätze der Patienten mit Herzrhythmusstörungen im Risikozeitraum, die vor der Impfung einen positiven SARS-CoV-2-Test aufwiesen, nach Impfstofftyp und -dosis.
Das Risiko von Herzrhythmusstörungen war nach der ersten Dosis von ChAdOx1 (IRR 0,95, 95 % KI 0,92, 0,97 nach 1–7 Tagen und über die folgenden Zeiträume) und BNT162b2 (IRR 0,79, 95 % KI 0,76, 0,81 nach 1–7 Tagen) verringert und über die folgenden Zeiträume) und nach einer zweiten Dosis von ChAdOx1 (IRR 0,84, 95 %-KI 0,82, 0,87 nach 1–7 Tagen; IRR 0,97, 95 %-KI 0,94, 0,99 nach 8–14 Tagen) und BNT162b2 (IRR 0,85, 95 %-KI 0,83, 0,88 nach 1–7 Tagen; IRR 0,95, 95 %-KI 0,92, 0,98 nach 8–15 Tagen).
Es bestand ein erhöhtes Risiko für Herzrhythmusstörungen nach einer zweiten Dosis von mRNA-1273 (IRR 1,93, 95 % KI 1,25, 2,96 nach 1–7 Tagen) und nach 1–7 Tagen (IRR 11,73, 95 % KI 11,33, 12,14), 8–14 Tage (IRR 6,57, 95 % KI 6,30; 6,85), 15–21 Tage (IRR 2,30, 95 % KI 2,15; 2,45) und 21–28 Tage (IRR 1,67, 95 % KI 1,55; 1,80) nach einem SARS -CoV-2 positiver Test.
In den 1–28 Tagen nach der Impfung fanden wir ein verringertes Risiko für Herzrhythmusstörungen in Verbindung mit einer ersten Dosis von ChAdOx1 (IRR 0,94, 95 %-KI 0,93, 0,96) und BNT162b2 (IRR 0,89, 95 %-KI 0,87, 0,90) und folgenden eine zweite Dosis von ChAdOx1 (IRR 0,95, 95 % KI 0,94; 0,96) und BNT162b2 (IRR 0,95, 95 % KI 0,93, 0,96). Nach einer zweiten Dosis mRNA-1273 (IRR 1,46, 95 % KI, 1,08, 1,98) und einem SARS-CoV-2-positiven Test (IRR 5,35, 95 % KI 5,21, 5,50) bestand ein erhöhtes Risiko für Herzrhythmusstörungen.
Diskussion
Dies ist die bisher größte Studie zu akuten kardialen Ereignissen nach einer SARS-CoV-2-Impfung oder -Infektion der ChAdOx1-Impfstoff.
Unsere Ergebnisse sind für die Öffentlichkeit, Kliniker und politische Entscheidungsträger relevant. Erstens gab es einen Anstieg des Myokarditisrisikos innerhalb einer Woche nach Erhalt der ersten Dosis sowohl des Adenovirus- als auch des mRNA-Impfstoffs und ein höheres erhöhtes Risiko nach der zweiten Dosis beider mRNA-Impfstoffe. Im Gegensatz dazu fanden wir keine Hinweise auf ein erhöhtes Risiko für Perikarditis oder Herzrhythmusstörungen nach der Impfung, außer in den 1–28 Tagen nach einer zweiten Dosis des mRNA-1273-Impfstoffs. Zweitens bestand in derselben Population ein höheres Risiko für Myokarditis, Perikarditis und Herzrhythmusstörungen nach einer SARS-CoV-2-Infektion. Drittens war das erhöhte Myokarditisrisiko nach der Impfung bei Personen unter 40 Jahren höher. Wir schätzten, dass zusätzliche Myokarditis-Ereignisse im Monat nach der Impfung zwischen 1 und 10 pro Million Personen lagen, was wesentlich niedriger war als die 40 zusätzlichen Ereignisse pro Million Personen, die nach einer SARS-CoV-2-Infektion beobachtet wurden.
